Anna Bertin
Chiara Chiappero

Sistema anaerobico e alattacido
Durante la contrazione muscolare il primo substrato energetico utilizzato dal muscolo scheletrico è l'adenosin trifosfato; tuttavia la quantità di ATP (80-100g per un individuo di 70 Kg) immagazzinata nel muscolo può far fronte ad uno sforzo di un solo secondo.
Successivamente il muscolo utilizza la fosfocreatina (PC), un accumulatore di energia situato nel citosol la cui concentrazione è circa 4-6 volte maggiore di quella dell'ATP e la cui autonomia energetica raggiunge i 3-5 secondi.
Depositi muscolari : concentrazioni
ATP 25 mM (normale) 17mM (fatica)
PC 85mM (normale) 5 mM (fatica)
L'utilizzo di queste due molecole è tipico delle fibre muscolari bianche. In seguito il muscolo impiega tre minuti per ritornare alle concentrazioni iniziali.
Sistema anaerobico lattacido
Quando uno sforzo muscolare si protrae oltre i 10 secondi, per ottenere l'energia necessaria vengono intaccati i depositi di glicogeno presenti nel muscolo e nel fegato tramite la glicogenolisi .
Tramite la glicolisi il glucosio viene demolito in due molecole di piruvato. La maggior parte dell'energia ottenuta viene conservata accoppiandola alla fosforilazione di quattro molecole di ADP ad ATP.
Nella sesta delle dieci tappe che compongono la glicolisi l'aldeide 3-fosfoglicerica viene ossidata a 1-3 bifosfoglicerato grazie a due molecole di NAD ossidato (NAD+) che funge da accettore di idrogenioni (H+). Il NAD viene quindi ridotto a NADH.
La resa energetica è di 2 ATP e 2 NADH per molecola di glucosio,in quanto due molecole di ATP sono state utilizzate nella fase preparatoria della glicolisi.
A questo punto, se vogliamo che l'energia continui ad essere generata attraverso la glicolisi dobbiamo preoccuparci di rigenerare il NAD ossidato (NAD+), che altrimenti verrebbe rapidamente depauperato fino ad esaurirsi. Quando la disponibilità di ossigeno è sufficiente la riossidazione del NAD ridotto è affidata al ciclo di Krebs (fosforilazione ossidativa mitocondriale), con consumo di ossigeno, formazione di acqua e sintesi di ATP. Quando invece l'ossigeno scarseggia, il piruvato che non entra nel ciclo di Krebs viene ridotto ad acido lattico per opera dell'enzima lattato deidrogenasi.
FERMENTAZIONE LATTICA
La fermentazione lattica è il sistema energetico utilizzato dai tessuti muscolari nelle attività che richiedono forza e resistenza per un tempo attorno al minuto(il culmine è raggiunto mediamente tra i 40 e i 45 secondi) e in quegli esercizi in cui la richiesta energetica è superiore alle normali disponibilità aerobiche delle cellule muscolari.
Lattato deidrogenasi

La lattato deidrogenasi (o LDH) è un enzima appartenente alla classe delle ossidoreduttasi.
E' un tetramero formato da due tipologie di monomeri: il tipo H (H dall'inglese heart), maggiormente presente nel cuore, e il tipo M, caratteristico del muscolo. Dalla diversa composizione monomerica, si hanno cinque forme isoenzimatiche: LDH1, LDH2, LDH3, LDH4, LDH5 che differiscono tra loro per composizione strutturale, proprietà biochimiche e diffusione tissutale.
- LDH1 è prevalente nel miocardio e nei globuli rossi. Presente anche nella corteccia renale e nel muscolo scheletrico.
- LDH2 è prevalente nel miocardio e nelle emazie, oltre ad essere presente nel pancreas, corteccia renale, polmone e muscolo scheletrico.
- LDH3 è presente in polmoni, placenta, muscolo scheletrico e pancreas.
- LDH4 si trova nella midollare renale, muscolo scheletrico, polmone e placenta.
- LDH5 è caratteristico del muscolo e del fegato. Presente anche nella midollare renale e nel pancreas.
Catalizza la seguente reazione:
ΔG°=-25 kJ/mole

ACIDO LATTICO

Nome IUPAC: acido 2-idrossipropanoico.
E’ un acido carbossilico e la sua formula chimica è C3H6O3 . La molecola dell'acido lattico è chirale, ne esistono pertanto due enantiomeri. L'enantiomero che compare nei cicli metabolici dei sistemi viventi è l'acido S-(+)-lattico o acido L-(+)-lattico
La sua deprotonazione dà origine allo ione lattato. Una volta prodotto, a pH fisiologico, l'acido lattico tende a dissociarsi quasi interamente nei due ioni: lo ione lattato e lo ione H+ .
Trasporto del lattato
Questa specie carica non può attraversare la membrana per diffusione semplice, ma richiede uno specifico sistema di trasporto fornito dai proton-linked monocaboxylate transporters (MCT).
Questi trasportatori catalizzano la diffusione facilitata del lattato in simporto con un protone. Il trasporto avviene quindi in favore di un gradiente di concentrazione di lattato e di pH. Sebbene il trasporto del lattato rappresenti il fenomeno quantitativamente più rilevante, bisogna ricordare che questi trasportatori possono trasportare anche altri importanti monocarbossilati metabolici, come il piruvato, i chetoacidi a catena ramificata e i corpi chetonici.
Gli MCT rappresentano una famiglia di proteine nella quale sono stati identificati almeno nove diversi membri nell’uomo.
MCT1 è ubiquitariamente espressa, ma è particolarmente evidente nel cuore e nelle fibre rosse del muscolo(fibre di tipo 1), dove è up-regolato in risposta a un aumento di lavoro, suggerendo un ruolo speciale nella ossidazione dell’acido lattico.
MCT4 è invece più evidente nel muscolo bianco(fibre di tipo 2) e altre cellule con un alto tasso di glicolisi, come le cellule tumorali e globuli bianchi, suggerendo che si esprime in cellule in cui predomina l’efflusso di acido lattico. Questa isoforma presenta la maggiore affinità per il lattato con una Km di circa 20 mM.
I meccanismi coinvolti nella regolazione dell'espressione delle diverse isoforme MCT devono ancora essere stabilite. Tuttavia, vi sono prove di splicing alternativo delle regioni 5'-e 3'-non tradotte e l'uso di promotori alternativi per alcune isoforme. Inoltre, MCT1 e MCT4 hanno mostrato di interagire specificamente con OX-47 (CD147), un membro della superfamiglia delle immunoglobuline con una singola elica transmembrana. Questa interazione sembra favorire l'espressione di MCT sulla superficie cellulare.
L’allenamento di endurance aumenta i livelli di MCT1 nelle fibre rosse. Sebbene una serie di studi suggeriscano che la capacità di trasporto di lattato/protoni possa essere migliorata con l’allenamento, è stata osservata una notevole variabilità interindividuale ed è possibile che vi sia una forte componente genetica nello sviluppo di questa capacità.
Fase di recupero
Grazie a questi trasportatori di membrana il lattato si riverserà immediatamente nel liquido interstiziale dal quale sarà captato dalle cellule muscolari non in situazione di accumulo (75% del lattato prodotto). La parte restante si riverserà nel sangue determinando il valore della lattacidemia (concentrazione di lattato nel sangue,valori basali 0.5-1.5 mEq/L); da qui si deduce come la misurazione del lattato ematico sia in grado di definire parzialmente il livello di accumulo cellulare. Infatti mentre la produzione di acido lattico nella cellula è direttamente proporzionale all'intensità dell'esercizio, la lattacidemia ha un andamento esponenziale.
Ciò è dovuto a:
1) gradiente di concentrazione del lattato che è scarso a bassi valori di velocità di consumo di O2 (consumo di ossigeno = intensità dell'esercizio)
2) scarsa attivazione dei trasportatori di membrana che fanno uscire il lattato a bassi valori di velocità di consumo di O2
3) diluizione del lattato in 5 litri di sangue quando questo è prodotto in bassa quantità.
Il lattato riversato nel sangue quindi sarà smaltito da altri muscoli oppure da fegato, cuore e reni.
Il lattato catturato dalle cellule epatiche viene ossidato di nuovo a piruvato ad opera della lattato deidrogenasi e quindi può essere:
• metabolizzato nella via gluconeogenica. In questo modo si dà vita al Ciclo di Cori.
• utilizzato per formare alanina con una reazione di aminazione
• decarbossilato per dare Acetil CoA

Shuttle del lattato
Le stesse fibre muscolare sono in grado di utilizzare il lattato sia durante lo sforzo muscolare sia durante la fase di recupero. In particolare è stato descritto un flusso di lattato dalle fibre di tipo 2 (fibre bianche) a quelle di tipo 1 (fibre rosse), in cui avviene l’ossidazione completa del lattato con produzione di CO2.
Lattacidemia
Rappresenta il bilancio tra la produzione del lattato, la sua diffusione nel torrente circolatorio e la sua eliminazione attraverso vari processi.
Durante la fase di recupero che segue un intenso sforzo lattacido, l’andamento della diminuzione della lattacidemia può essere descritta da una curva di smaltimento facente riferimento al tempo di dimezzamento delle concentrazioni ematiche.
 Ipotizzando un valore di lattacidemia di 20 mM, nell’individuo non allenato, questo tempo è di circa 15 minuti. Ciò significa che ci vorranno almeno 60 minuti per tornare ai valori basali.
Ipotizzando un valore di lattacidemia di 20 mM, nell’individuo non allenato, questo tempo è di circa 15 minuti. Ciò significa che ci vorranno almeno 60 minuti per tornare ai valori basali.
Nei soggetti allenati il tempo di dimezzamento è più breve e, a parità di valori di lattacidemia dopo sforzo, si possono raggiungere i valori basali in circa 30 minuti.
Lattacidemia in funzione del carico
Durante un esercizio a carichi crescenti si osserva che la lattacidemia tende a rimanere costante nei carichi iniziali. Ciò significa che con carichi di intensità bassa non si verifica un accumulo del lattato nel sangue; negli atleti praticanti sport di lunga durata si può anche osservare,al termine dei primi carichi di lavoro, una lieve diminuzione della lattacidemia rispetto ai valori basali.
Tale diminuzione avviene ad opera dell'attivazione dei sistemi di smaltimento del lattato che sono in questi atleti particolarmente efficienti, per cui l'equilibrio tra produzione e smaltimento viene e trovarsi a livelli di lattacidemia inferiori ai basali.
Con il progressivo aumento dell'intensità dell'esercizio si assiste ad un aumento della lattacidemia, ma solo a partire da una determinata intensità di esercizio.
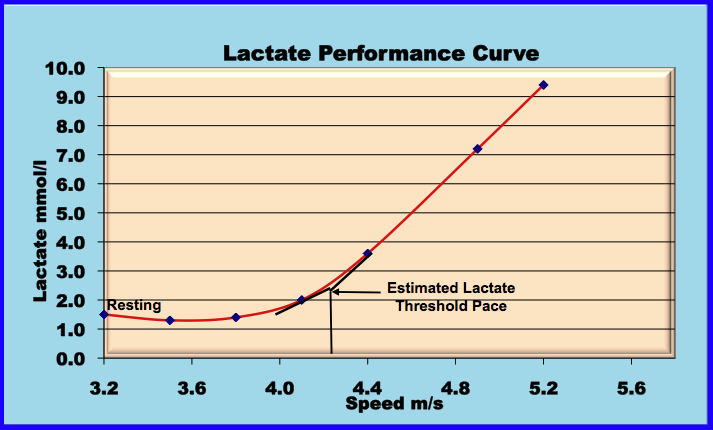
La relazione tra l’incremento del carico (potenza) e il livelli ematici di lattato viene rappresentata da una curva esponenziale.
Possiamo definire “soglia anaerobica” quell’intensità di lavoro a cui il lattato ematico raggiunge il valore di 4 mM durante prove di intensità progressivamente crescente.
FATICA
Al contrario del lattato,che non ha grande effetto, l’abbassamento del pH (acidosi) influenza notevolmente l’attività muscolare essendo coinvolto nel fenomeno della fatica, che si manifesta come diminuzione della forza muscolare, decremento della velocità di sviluppo della forza e rallentamento del rilasciamento.
In particolare l’accumulo di H+ diminuisce l’affinità della troponina per il calcio e la velocità dell’idrolisi di ATP, della formazione del complesso actina-miosina, della glicolisi e della glicogenolisi.
Occorre però ricordare che l’acido lattico non è, come si riteneva un tempo, l’unico responsabile dell’affaticamento muscolare; è infatti molto probabile che l’accumulo del fosfato derivato dalla scissione della fosfocreatina dia un contributo importante. L’ incremento della concentrazione di fosfato(normale 5 mM, fatica 90 mM) da un lato inibisce la liberazione del fosfato inorganico e quindi lo sviluppo di forza (power stroke), dall’altro diminuisce la sensibilità dell’apparato contrattile al calcio.

DOMS
I sintomi da presenza di acido lattico non sono da correlare con l’indolenzimento muscolare ad insorgenza ritardata, meglio noto con l'acronimo anglosassone D.O.M.S. (Delayed Onset Muscle Soreness), i cui effetti solitamente si palesano tra le 12 e le 72 ore circa dallo sforzo fisico intenso, perdurando anche per 5-6 giorni consecutivi, e sono attribuibili a microlesioni delle fibrocellule del muscolo scheletrico. L’affaticamento muscolare causato dall’acido lattico scompare infatti entro qualche ora.