| Author: Giulia Bertero & Mattia Paolo Doronzo |
Introduzione
La medicina rigenerativa rappresenta il santo Graal della medicina moderna e, pur essendo questo un campo di ricerca relativamente giovane ed incerto, significativi progressi sono stati fatti negli ultimi 20 anni. Nella trattazione che segue ho voluto portare alla vostra attenzione le potenzialità di uno studio di straordinaria portata pubblicato su Nature a fine 2013, e che permetterebbe di scrivere un nuovo capitolo nella storia della medicina rigenerativa cardiovascolare, offrendoci un valido strumento nella lotta ad una delle patologie cardiache più diffuse al mondo, che ogni anno colpisce mediamente circa 2 persone su 100 in Italia: l’Infarto.
Per Infarto del Miocardio (IMA) si intende la sindrome coronarica acuta dovuta all'ostruzione di una arteria coronaria a seguito della formazione di un trombo occludente con conseguente necrosi del tessuto miocardico, incapace di sopportare condizioni di ipossia anche per brevi tempi. Il tessuto miocardico non possiede la capacità autorigenerativa che caratterizza tessuti come la cute e le mucose, e gli eventi ischemici, conseguenti all’esposizione del tessuto ad un ambiente ipossico, portano alla sua sostituzione con tessuto fibrotico, compromettendo di conseguenza la funzionalità dell’organo e portando ad un’elevata mortalità.
Approcci Terapeutici alla Medicina Rigenerativa Cardiovascolare
Numerose strategie sono state testate per la messa a punto di terapie rigenerative cardiovascolari, come la somministrazione di cellule indifferenziate espanse in vitro, di proteine ricombinanti e il veicolo di “geni terapeutici” mediante DNA plasmidico o vettore virale. Tutti questi tipi di approccio hanno però portato risultati insoddisfacenti: le cellule indifferenziate hanno dimostrato un basso grado di attecchimento in vivo nel lungo termine; le proteine esogene somministrate hanno rivelato scarsa specificità per il tessuto cardiaco, un’emivita significativamente ridotta in vivo ed un’alta tossicità sistemica per somministrazione di elevati dosaggi; le terapie basate su un approccio genico hanno evidenziato un inadeguato controllo dell’espressione, basso grado di trasfezione, risposta immunitaria antivirale e rischio di integrazione del DNA nel genoma della cellula bersaglio, con conseguente rischio di tumorigenicità.
Provvidenziale è stato in questi termini il lavoro svolto da Derrick Rossi, il quale nel 2010 pubblicò un articolo nel quale descriveva la messa a punto di una nuova tecnica in grado di indurre la staminalità in cellule differenziate mediante la somministrazione in vitro di specifici modRna. Per modRna si intende un normalissimo mRna al quale vengono sostituite alcune basi e coniugate delle proteine che ne regolano l’espressione una volta entrato all’interno della cellula bersaglio. Per favorirne l’ingresso nella cellula, il modRna viene complessato con un “veicolo” di natura cationica che ne favorisce l’uptake mediante endocitosi, un processo costitutivo della cellula. La traduzione di tali modRna in proteine porta alla regressione della cellula differenziata ad uno stadio indifferenziato decisamente migliore rispetto a quello che si era finora riusciti ad ottenere mediante l’esposizione della cellula a determinati “cocktail” di molecole segnalatrici, e con una percentuale di successo notevolmente più elevata.
Se interessati all’argomento allego qui il link per l'articolo Highly efficient reprogramming to pluripotency and directed differentiation of human cells with synthetic modified mRNA e un Video di spiegazione riguardante la tecnica di riprogrammazione.
L’ideazione di un vettore nucleico che ci consente di indurre l’espressione di una qualsivoglia proteina in un qualsivoglia gruppo di cellule, e con una cinetica di produzione ben determinata, apre le porte a nuove possibilità terapeutiche. Nel comprendere tali potenzialità sta l’intuizione del team diretto da Kenneth Chien, che decise di provare ad utilizzare un modRna come vettore in vivo per indurre l’espressione di VEGF-A da parte delle cellule cardiache stesse. Perché proprio il VEGF-A? Andiamo per gradi…
Possibili Target Terapeutici
Nonostante il cuore sia privo di capacità rigenerativa, sulla superficie epicardica sono presenti delle cellule progenitrici cardiache multipotenti chiamate ISL1+ progenitors. Queste cellule multipotenti sono dirette discendenti delle stesse Embryonic Stem Cells (ESC) (vengono infatti denominate hESC-derived ISL1+progenitors) che durante il periodo di sviluppo fetale del cuore si differenziano in Endothelial Cells (EC), Smooth Muscle Cells (SMC) e Cardiomyocites (CM), dando origine all’intero tessuto cardiaco. È stato dimostrato in modelli murini che, in seguito ad infarto del miocardio indotto per chiusura dell’arteria coronaria, le ISL1+ progenitors si attivano entro le 48 ore dalla legatura. Esse però non vanno a ricostruire il tessuto miocardico in necrosi, anzi, lo sostituiscono differenziando in fibroblasti ed andando così a costituire uno spesso strato di tessuto fibrotico cicatriziale, compromettendo così la funzionalità cardiaca. Queste cellule progenitrici perdono dunque nel cuore sviluppato la capacità di mobilizzarsi, entrare nel tessuto miocardico e differenziare in linee cellulari cardiovascolari come facevano nel cuore fetale, rimanendo invece nello strato epicardico superficiale e differenziano piuttosto in fibroblasti e mio-fibroblasti in seguito ad un evento ischemico.
Studi recenti hanno dimostrato il ruolo centrale di alcuni fattori paracrini nella regolazione dell’attività di queste cellule progenitrici durante lo sviluppo fetale del cuore, ed il VEGF-A sembra essere uno dei più importanti. In particolare, lo stesso team di Chien ha messo in evidenza l’effetto che il VEGF-A ha sulle stesse ISL1+ progenitors [riportate in Figura come WT1+] nell’indurne la proliferazione ed il “Cell-fate decision” in direzione Epiteliale (EC) e, anche se in termini quantitativamente inferiori, in Cardiomiociti (CM) in vitro.

Per maggiori informazioni consultate il seguente articolo Driving vascular endothelial cell fate of human multipotent Isl1+ heart progenitors with VEGF modified mRNA
Una Nuovo Approccio Terapeutico
Il team diretto da Chien decise dunque di verificare se si potesse riuscire ad ottenere lo stesso risultato anche “in vivo”. Da qui nacque l’idea di utilizzare come vettore genico un modRna che inducesse la produzione di VEGF-A da parte delle stesse cellule che compongono il tessuto cardiaco, così da ottenere in vivo lo stesso effetto di differenziazione delle ISL1+ progenitors finora ottenuto solamente "in vitro". Infatti, se si riuscisse ad indurre nella zona colpita da infarto la proliferazione e la differenziazione di queste cellule in cellule endoteliali, ne conseguirebbe un fenomeno di angiogenesi che contribuirebbe a ristabilire l’apporto ematico alla zona colpita da ipoperfusione ipossica, favorendo il recupero di funzionalità del tessuto cardiaco. La verifica di queste ipotesi ha portato a risultati entusiasmanti.
Come consuetudine, il team decise di verificare tali ipotesi partendo da un modello murino. Innanzitutto cominciarono dal verificare l’effettiva efficacia di trasfezione cellulare "in vivo" con modRna. Con grande sorpresa risultò non solo che questa modalità di trasfezione aveva una tossicità minima per le cellule, ma che si riusciva anche ad infettare, con un’efficienza dalle 10 alle 40 volte maggiore rispetto ai metodi precedenti, i cardiomiociti e le cellule muscolari scheletriche di ratto, cellule notoriamente difficili da trasfettare. Inoltre i modRna utilizzati sono sintetizzati in modo tale da evitare il riconoscimento da parte del sistema immunitario dell’mRna che li compone come mRna virale. In questo modo si riesce ad evitare la risposta immunitaria dell’organismo contro le cellule trasfettate, risposta che costituisce uno dei principali problemi nell’utilizzo di vettori virali in vivo.
In seguito legarono la coronaria di un topo, inducendo l’infarto, e procedettero ad iniettare il modRna codificante per il VEGF-A direttamente nella zona di miocardio colpita dall’ischemia. Infine analizzarono i dati relativi alla sopravvivenza a breve e lungo termine dei topi trattati con il modRna confrontandoli con quelli dei topi lasciati senza trattamento. I risultati furono a dir poco sorprendenti. Per quanto riguarda gli effetti a breve termine (4 settimane), si è visto che il trattamento con modRna non solo aumentava la vascolarizzazione nella zona colpita da infarto, ma riduceva anche l’estensione dell’area danneggiata. La figura che segue mette bene in evidenza questi due aspetti, mostrando il cuore infartuato di ratto prima (sinistra) e dopo (destra) il trattamento.
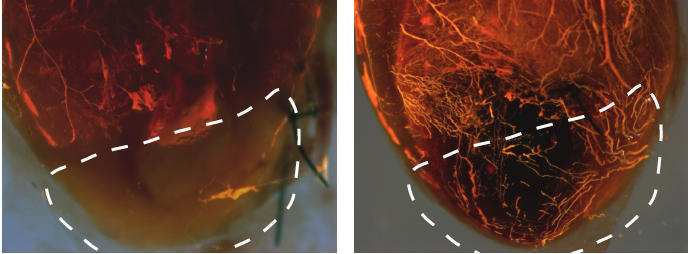
Di seguito allego anche una Risonanza magnetica (MRI) effettuata a 21 giorni di distanza dal trattamento. Il video rende bene l'idea del recupero effettuato dal punto di vista cinetico dall'area interessata dall'infarto. I risultati più eclatanti però si registrano sul lungo termine, come potete vedere nella figura riportata di seguito:
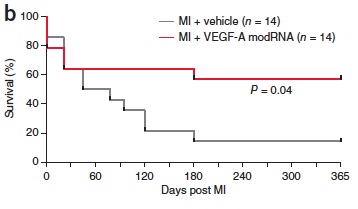
Mentre la sopravvivenza del caso-controllo ad un anno dall’infarto si attestava al 20%, la sopravvivenza dei topi trattati con modRna risultava aumentata al 60%.
Verifiche successive dimostrarono che i benefici ottenuti con questa terapia erano attribuibili all’effetto esercitato dal VEGF-A sulle ISL1+ progenitors. Marcando tali cellule, i ricercatori hanno potuto seguire il loro comportamento nel tempo, ed attestare non solo che la loro esposizione al VEGF-A ne favorisce la proliferazione, ma che ne induce anche la mobilizzazione dalla superficie epicardica verso gli strati più interni, una capacità persa da queste cellule in seguito allo sviluppo fetale del cuore. Una volta migrate nel subendocardio queste differenziano in cardiomiociti e, per la maggior parte, in cellule endoteliali, favorendo la vascolarizzazione degli strati più interni del miocardio.
Il successo della vascolarizzazione è soprattutto dovuto alle modalità di secrezione del VEGF-A da parte delle cellule trasfettate. Anche la trasfezione con Dna plasmidico codificante per lo stesso VEGF-A porta ad una marcata angiogenesi, ma con una differenza rispetto alla vascolarizzazione ottenuta tramite modRna. I capillari che si vengono a formare in seguito alla trasfezione con modRna sono perfettamente funzionanti, mentre quelli che si originano dalla trasfezione con Dna plasmidico sono troppo permeabili. Questo porta alla formazione di edema nel tessuto cardiaco, con conseguente aumento della mortalità. Questo è in parte dovuto alla diversa modalità di secrezione di VEGF-A ottenuta con i due metodi, ed illustrata in Figura "l":

Il modRna porta ad una modalità di secrezione del VEGF-A definita “pulse-like”, ovvero viene rapidamente raggiunto un picco di secrezione molto elevato entro le 6 ore dalla somministrazione, il quale diminuisce altrettanto velocemente. La produzione di VEGF-A mediata dal Dna plasmidico raggiunge invece un picco di secrezione molto più basso entro le 72 ore, e che si mantiene elevato nel tempo scendendo molto lentamente. Se ne deduce quindi che è cruciale per la formazione di capillari ben funzionanti anche la modalità ed il tempo di esposizione delle ISL1+ progenitors a tali fattori angiocrini: un’esposizione prolungata ad essi porta alla formazione di capillari eccessivamente permeabili, mentre un’esposizione breve ed intensa ne favorisce il giusto sviluppo.
Modified mRNA directs the fate of heart progenitor cells and induces vascular regeneration after myocardial infarction
Considerazioni
Questo studio ci offre quindi un’interessante prospettiva terapeutica per una delle patologie cardiovascolari più diffuse, ponendo le basi per la sperimentazione sull’uomo. Questa modalità di intervento sembra aver superato le difficoltà ed i limiti delle tecniche passate, riducendo i rischi per il paziente ed accendendo la speranza di una sua applicazione in altri ambiti della medicina rigenerativa.