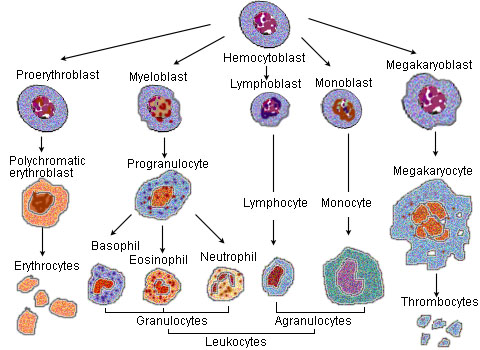
Blood cells are produced in the bone marrow (W)

Some hematopoietic stem cells are more equal than others 2010

Homogeneous versus heterogeneous HSC populations. (A) Traditional scheme of a uniform HSC population in which each cell has a similar propensity to give rise to different lineage-committed progeny (top). Propensities to generate different lineages are symbolized by different colors. The composition of pool of differentiated cells (bottom) is determined by different production rates beyond the stem cell level (indicated by thickness of arrows). (B) New findings suggest that the propensities of different HSCs to give rise to different lineages are fixed, so the lineage mix in the periphery may be influenced by the composition of the HSC pool. Morita et al. (2010) show that different lineage-biased HSCs can be enriched using the surface marker CD150.